2025年7月10日,創新藥港股上市公司中國抗體發布,其全球首創新藥SM03(舒西利單抗,Suciraslimab)針對系統性紅斑狼瘡(SLE)的臨床前研究取得突破性結果。
SM03作為靶向CD22靶點的人源化單克隆抗體,憑借“雙通路精準調控+多器官保護效應”的獨特優勢,有望填補SLE治療中“長期安全與多器官保護”的未滿足需求,為全球患者提供療效更佳更安全的全新治療方案。
1 高速發展與擴容的系統性紅斑狼瘡藥物市場
系統性紅斑狼瘡(SLE)是一種慢性、自身免疫性疾病。這意味着身體的免疫系統錯誤地攻擊自身的健康組織和器官,引起炎症和損傷。
SLE可以影響身體的多個系統和器官,常見受累部位包括:皮膚和黏膜(面頰部蝴蝶狀皮疹)、關節(關節炎或關節痛是最常見症狀之一)、腎病、貧血、頭痛、癫痫、認知障礙、情緒變化、胸膜炎、心包炎、以及胸痛、呼吸困難等。且不同患者的症狀差異極大,沒有兩個患者的表現是完全相同的。
全球SLE患者超過500萬,單是中國患者規模就超過百萬,且其中50%患者會進展為狼瘡性腎炎(終末期腎病風險高)。然而現有的傳統藥物治療(糖皮質激素、免疫抑制劑)存在顯著局限,長期使用副作用大,療效随時間衰減。
與國際水平相比,中國SLE治療和管理仍存在差距。CSTAR的數據顯示,中國僅有0.76%的SLE患者能夠達到無藥物治療疾病完全緩解,而國際水平已從1982年的2.5%升至2019年的6%;此外,中國SLE患者隊列中,僅2.47%能夠達到藥物治療臨床緩解,而國際上已從2014年的2.1%升至2019年的22.9%。
與此同時,全球SLE的治療藥物市場也正在經曆前所未有的高速發展與擴容,而中國的潛在增速高于全球均值。弗若斯特沙利文(Frost & Sullivan)預測,到2037年,全球SLE治療市場規模将超過63.7億美元。中國作為SLE患者數量最多的國家之一,預計到2030年患者人數将接近110萬,市場潛力巨大。現有重磅藥物如貝利尤單抗的年銷售額已突破17億美元,并預計将持續增長,這充分證明了SLE市場巨大的商業價值。
臨床上,傳統治療方法主要依賴糖皮質激素和廣譜免疫抑制劑,這些療法類似“地毯式轟炸”,在抑制過度激活的免疫反應時,也無差别地壓制了正常的免疫功能,導緻感染風險增加、代謝紊亂等一系列副作用。
随着生物技術的發展,靶向治療為SLE帶來了新的曙光。貝利尤單抗、泰它西普等生物制劑的上市,标志着SLE治療進入了精準時代。雖然這些藥物都能夠緩解患者症狀,提高生活質量,但是都不能有效地根治或維持長期緩解。因此,通過創新療法實現長期緩解乃至治愈,仍是SLE治療領域亟需解決的未滿足需求。
由中國抗體(03681.HK)開發的舒西利單抗(Suciraslimab, SM03),憑借其獨特的雙重作用機制和在臨床前研究中展現出的巨大潛力,成為SLE創新藥賽道中備受矚目的候選者。
2 系統性紅斑狼瘡的緻病機理與現有的治療方式
系統性紅斑狼瘡(SLE)的免疫學特征是抗核抗體(antinuclear antibodies,ANA)的産生,它們針對DNA、RNA和與RNA結合的蛋白質,導緻免疫複合物(immune complex,IC)的沉積、炎症反應、細胞因子釋放和器官損傷。并且常伴有狼瘡性腎炎(LN),LN是SLE最嚴重的并發症之一,導緻腎髒炎症和功能受損。
B細胞是緻病性抗核抗體的來源,因此靶向B細胞的療法一直是系統性紅斑狼瘡(SLE)研發的重要方向,并已催生多個獲批藥物。此外T細胞由于是驅動B細胞産生緻病性抗體、以及直接參與組織炎症的核心,因此抑制過度活躍的T細胞反應,也是當前的主要療法之一。
其中利妥昔單抗直接靶向B細胞上的受體CD20,導緻CD20+的B細胞凋亡。但是異常B細胞所産生的抗核抗體的長壽命漿細胞和漿母細胞上無CD20表達。而貝利尤單抗及泰它西普可通過阻斷BLyS與其受體的相互作用,從而阻止異常B細胞分化成為漿細胞,但往往無法完全阻止所有B細胞分化。而關于LN的治療,Synbiose研究表明,貝利尤單抗和利妥昔單抗在減少蛋白尿和改善腎組織病理方面的效果有限,且B細胞長期耗竭顯著增加感染風險,有概率影響患者長期免疫安全。
針對這些問題的改善方式包括CAR-T療法以及雙抗療法等。其中,針對CD19靶點的CAR-T療法有望達到深度清除緻病性B細胞的效果,觸發免疫“重置”,實現完全緩解疾病,使患者恢複正常生活。但其缺點是成本近乎“天價”:在美國每針平均30~50萬美元,而中國則需百萬人民币以上,患者的可及性非常低。
雙抗療法目前有CD3xCD20與CD47xCD20兩種。其中,前者引入T細胞高效清除變異的B細胞,而後者則激活巨噬細胞對變異B細胞的識别而将其消滅。兩者都能夠高效地清除緻病B細胞,但前者會造成T細胞耗竭,損傷患者免疫系統;而後者有可能使正常B細胞數量減少,因而兩者都有較高的感染風險。此外,由于CD47也會在部分紅細胞與血小闆表達,因此CD47療法也會導緻貧血的副作用。
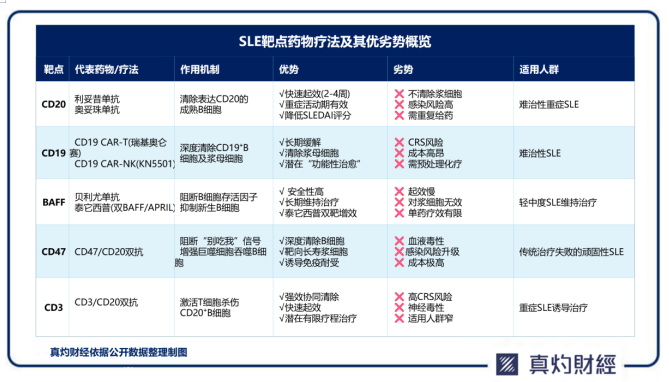
此外,目前所有單向影響B或T細胞通路的治療手段臨床上對SLE引起的腎炎及蛋白尿等效果不佳。原因在于狼瘡性腎炎的緻病機理中,免疫複合物處于核心地位。而不論是B細胞還是T細胞的靶向治療都無法清除腎小球内業已沉積的免疫複合物。此外,腎髒存在獨立于全身的免疫環路,導緻B/T細胞靶向藥物難以穿透腎髒組織并抑制局部炎症。
相比之下,SM03 作為一款以B細胞為中樞節點,其設計理念則旨在通過一個分子實體,同時幹預兩個關鍵緻病軸,通過靶向調控該關鍵免疫樞紐進而調節其他免疫細胞及系統性自身免疫炎症的創新藥物,有望打破傳統治療瓶頸,在安全性與療效之間實現更優平衡,提升SLE尤其LN患者的治療效果。
3 舒西立單抗(SM03)治療SLE原理與優勢
SM03是一款靶向CD22的人源化單克隆抗體。CD22是B細胞表面的一個抑制性共受體,其功能在于防止B細胞的過度激活。
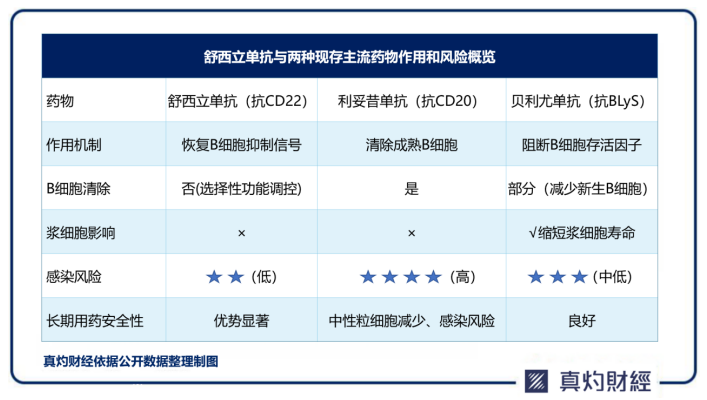
與靶向CD20的利妥昔單抗不同,SM03的核心機制并非清除B細胞,而是作為一種B細胞調節劑。它通過與CD22結合,改變其構象并招募抑制性分子,從而抑制B細胞的過度活化和自身抗體的産生。
這種非耗竭性的調節方式,在抑制緻病性B細胞活性的同時,保留了B細胞的正常免疫監視功能,從而顯著降低了嚴重感染的風險,并可能更好地保留患者對疫苗的應答能力。這構成了SM03相較于利妥昔單抗的“2.0”升級優勢。
更為關鍵的是,SM03展現出了超越傳統B細胞靶向藥物的雙重作用機制。
臨床前研究顯示,SM03 可對 B 細胞發揮免疫調節作用,實現對 B 細胞的抑制;而 B 細胞(同時可作為抗原呈遞細胞)能與其他免疫細胞(如T細胞, 樹突狀細胞, 漿細胞樣樹突狀細胞和巨噬細胞)發生交叉對話,進而抑制其他免疫細胞功能。這一點在系統性紅斑狼瘡(SLE)動物模型中得到證實:經SM03治療後,系統性紅斑狼瘡(SLE)模型動物的抗雙鍊DNA(anti-dsDNA)抗體水平顯著下降,且無需誘導B細胞耗竭即達到與B細胞耗竭療法藥物利妥昔單抗相當的療效。需特别強調的是:anti-dsDNA抗體作為SLE的核心緻病性自身抗體,在約70%的患者中呈陽性;這些抗體通過形成循環免疫複合物沉積于腎髒、皮膚及關節等多器官,激活補體系統并招募炎症細胞浸潤,直接加劇全身性組織損傷——尤其是驅動狼瘡性腎炎(LN)的病理進程。
在改善腎髒終點方面,直接比較研究證實SM03對蛋白尿及腎髒組織病理損傷的逆轉效果顯著優于利妥昔單抗。這一突破性優勢表明:SM03不僅有效降低緻病性anti-dsDNA水平,更能通過精準調控B細胞與T細胞間的異常交叉互作,抑制T細胞過度活化及其介導的腎髒炎症級聯反應,從而阻斷了傳統B細胞耗竭或增殖抑制類藥物無法解決的腎髒損傷惡性循環。
SM03的獨特機制在于其以非耗竭性方式重塑免疫穩态:通過糾正B細胞-T細胞病理性互作樞紐,選擇性抑制T細胞異常活化與下遊緻炎信号;進而同步減少免疫複合物在腎髒的沉積以直接改善腎小球濾過屏障功能;最終顯著緩解狼瘡性腎炎(LN)相關的蛋白尿及腎小管間質纖維化。此外,SM03已在臨床應用中展現卓越的長期安全性,患者耐受性良好,為慢性治療提供了關鍵保障。
SM03憑借其獨特的分子設計及作用機理,巧妙整合了雙重協同治療機制:既能通過非耗竭性免疫調節作用精準糾正B細胞功能異常,逆轉其與T細胞的病理性互作,協同抑制B細胞過度活化及T細胞異常增殖與緻炎因子分泌;又能通過調控B細胞-T細胞免疫樞紐,幹預樹突細胞、單核細胞等其他免疫細胞的活化級聯,從而多維度抑制系統性自身免疫炎症——這種多靶點協同作用突破了現有B細胞靶向療法(如利妥昔單抗)對終末器官損傷修複的局限性。
基于上述機制,SM03在狼瘡性腎炎(LN)治療中展現出突破性療效:通過重塑多免疫細胞網絡穩态,其改善蛋白尿及腎小球病理損傷的效果顯著優于傳統B細胞耗竭或增殖抑制類藥物,為逆轉不可逆性腎髒損傷提供了新策略。
腎髒是SLE最常攻擊的器官之一,約40%至60%的患者會發展為狼瘡性腎炎(LN),這是導緻SLE患者死亡和終末期腎病的主要原因。在LN這一“硬骨頭”面前,現有生物制劑的療效普遍不盡如人意:利妥昔單抗對腎髒沒有獲益,而貝利尤單抗在LN中的療效較弱。
在保護腎髒方面,SM03又成了那個潛在破局者。臨床前研究證實,SM03不僅能有效減少蛋白尿——這是衡量腎髒損傷的關鍵指标,還能改善腎髒組織的病理學表現。獨特的腎髒保護作用,使其在競争格局中脫穎而出,有望填補LN治療領域的巨大空白。
對于LN占優勢的SLE患者且自身抗體陽性的患者亞群,以及對現有生物制劑(如利妥昔單抗、貝利尤單抗)治療失敗的難治性患者,SM03的雙重機制提供了極具吸引力的治療選擇。
注:本報告所述研究結果摘錄自持續進行的研究。詳細的方法論、完整數據及分析将提交學術期刊發表。
4 廣闊的商業化前景
對于SM03的獨特原理與廣泛的适應症,中國抗體主席、執行董事兼首席執行官梁瑞安博士表示:"SM03有望成為系統性紅斑狼瘡(SLE)領域的全球首創且同類最優療法。”
中國抗體聚焦 “免疫疾病創新療法” 研發,以SM17和SM03為核心構建多靶點、多适應症管線。全球首創新藥SM17(靶向IL-25 受體),近期在特應性皮炎領域取得突破性臨床研究進展,在快速起效和止癢上取得巨大競争優勢;SM03(CD22單抗)除用于SLE、RA外,臨床前研究顯示其在幹燥綜合征、類天疱瘡等B細胞驅動疾病中潛力顯着,未來可拓展至神經免疫領域(如阿爾茨海默症,相關機制研究已發表)。憑借多個創新管線的組合,中國抗體已經逐漸形成“協同研發+全球化拓展”生态。
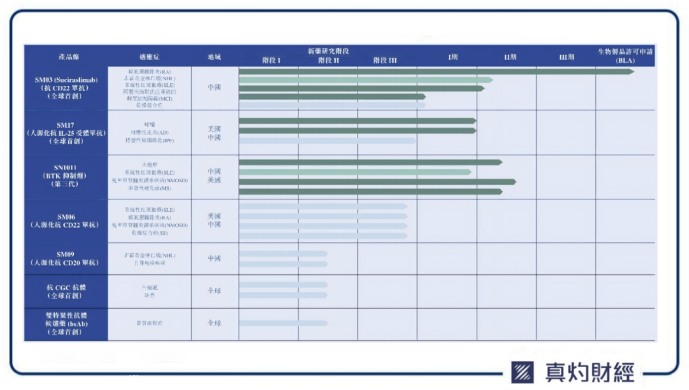
進入2025年,全球創新藥交易授權領域漸趨恢複往日的繁榮,國際醫藥大廠對于收購創新藥授權的出價敢于提出更高的價格。面對一個需求巨大且仍在增長的全球SLE市場,SM03完全有潛力成為該領域的下一個重磅藥物。
如果SM03在關鍵性臨床試驗中能成功驗證其在LN治療上的價值,不僅将為全球數百萬SLE患者帶來福音,也将為中國抗體制藥開啟一個全新的商業化篇章。







